비리어드정, 비리어드정 복용, 비리어드정 부작용, 비리어드정 이상반응, 비리어드정 주의사항

아프면 병원에 가고, 병원에 가서 검사를 받고, 의사가 처방한 약을 먹잖아요?
그러다보면 문득 이 약이 뭘까? 하는 생각이 들 때가 있더라고요.
내 몸에 맞는 약인지, 부작용은 없는지, 어디에 작용하는 약인지 등..
궁금한 데 어디가서 물어볼 수도 없고, 그렇다고 안 먹을 수도 없고.
그래서 인터넷상에 올라온 약 종류에 대한 글을 적으려고 해요.
의사나 약사가 아니라서 글이 정확하지 않다는 점 유의하시고 읽어주세요.
(가장 정확한 방법은 의사나 약사와 얘기하는 거예요~)
조금이나마 포스팅을 읽는 분들께 도움이 됐으면 좋겠네요 :)
출처는 https://terms.naver.com/medicineSearch.nhn

https://terms.naver.com/entry.nhn?docId=2125905&cid=51000&categoryId=51000
비리어드정
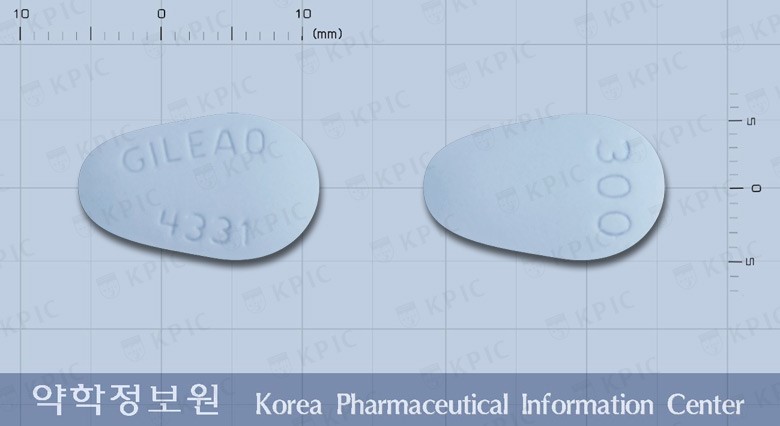
[외형정보] · 성상 : 연한 청색의 아몬드 모양의 필름코팅정 · 제형 : 필름코팅정 · 모양 : 물방울형 · 색상 : 파랑 · 식별표기 : (앞)GILEAD 4331, (뒤)300 [성분정보] 테노포비르디소프록실푸마레이트 300mg [저장방법] 기밀용기, 실온(1-30℃)보관 [효능효과] 1. HIV-1 감염 성인 및 12세 이상의 소아에서 HIV-1감염의 치료를 위해 다른 항레트로바이러스제제와 병용투여한다. 이 약은 테노포비르 함유 복합제제와 함께 복
terms.naver.com
비리어드정
[ Viread Tab. ]
식약처 분류 : 항병원생물성 의약품 > 화학요법제 > 기타의 화학요법제
구분 : 전문 의약품
제조(수입) 업체명 : 길리어드사이언스코리아
제조·수입 구분 : 수입
보험코드 : 625900040
외형정보
· 성상 : 연한 청색의 아몬드 모양의 필름코팅정
· 제형 : 필름코팅정
· 모양 : 물방울형
· 색상 : 파랑
· 식별표기 : (앞)GILEAD 4331, (뒤)300
이상반응
1) 임상 시험에서의 이상반응
임상 시험은 광범위하고 다양한 조건에서 시행되므로, 약물의 임상 시험에서 관찰되는 이상반응 비율을 다른 약물의 임상 시험에서의 이상반응 비율과 직접적으로 비교할 수 없으며, 실제로 관찰되는 비율에 반영되지 않을 수도 있다.
HIV-1 감염 환자에 대한 임상 시험
12,000명 이상의 환자가 이 약 단독 또는 기타 항레트로바이러스 의약품과 병용하여 임상시험과 접근성 확대 프로그램(expanded access program)을 통해 28일에서 215주까지 치료를 받았다. 총 1,544명의 환자가 임상 시험에서 1일 1회 테노포비르 디소프록실 푸마르산염 300mg을 투약 받았으며 11,000명 이상의 환자가 접근성 확대 프로그램을 통해 이 약을 투약 받았다.
세 건의 대규모 대조 임상 시험에서 발진, 설사, 두통, 통증, 우울증, 무력증 및 구역질이 가장 흔한 이상반응(발병률 10% 이상, 등급 2-4)으로 확인되었다.
가. 치료 경험이 없는 HIV-1 감염 성인 환자
시험 903 - 치료 후 발생한 이상반응 : 144주 동안 테노포비르(N=299) 또는 스타부딘(N=301)을 라미부딘 및 에파비렌즈와 병용하여 치료받은 600명의 치료 경험이 없는 환자에 대한 이중맹검 비교 시험에서 나타난 가장 흔한 이상반응은 경증 내지 중등도의 위장장애 및 현기증이었다.
경증의 이상반응(등급 1)은 두 치료군에서 비슷한 빈도로 발생했으며 현기증, 설사 및 구역질 등이 이에 해당한다. 중등도 내지 중증의 선정된 치료 후 발생한 이상반응이 표 2에 요약되어 있다.
표 2 시험903(0-144주)에서 5% 이상 발생이 보고된 치료 관련 이상반응a(등급 2-4)

a. 이상반응 빈도는 시험약과의 상관관계와 무관하게 모든 치료 후 발생한 이상사례를 기반으로 한다.
b. 지방이영양증은 프로토콜에서 정의된 증후군이 아니라 시험자가 기술한 다양한 이상사례를 의미한다.
c. 말초 신경병증은 말초 신경염 및 신경병증을 포함한다.
d. 발진 반응에는 발진, 가려움증, 반구진발진, 두드러기, 수포성 발진 및 농포성발진 등이 있다.
임상검사치 이상 : 공복상태 중 콜레스테롤 및 트리글리세리드 증가가 테노포비르 그룹(19% 및 1%)에 비해 스타부딘 그룹(40% 및 9%)에서 더 흔하게 발생한 점을 제외하고, 이 시험에서 두 그룹에서 관찰된 임상검사치 이상은 비슷한 빈도로 발생했다. 등급 3과 4 실험실적 결과 요약 내용은 표 3에 나와 있다.
표 3 시험 903(0-144주)에서 이 약 치료군 중 1% 이상 보고된 등급 3/4 임상검사치 이상

시험 934 - 치료 후 발생한 이상반응 : 항레트로바이러스 치료 경험이 없는 511명의 대상자가 에파비렌즈와 테노포비르 + 엠트리시타빈의 병용요법(N=257) 또는 에파비렌즈와 지도부딘/라미부딘 복합제의 병용요법(N=254)으로 치료받았다. 이 시험에서 관찰된 이상반응은 치료 경험이 있거나 치료 경험이 없는 대상자를 대상으로 한 이전 시험과 일반적으로 일치했다(표 4).
표 4 시험 934(0-144주)에서 5% 이상 발생이 보고된 치료 관련 이상반응a (등급 2-4)

a. 이상반응 빈도는 시험약과의 상관관계와 무관하게 모든 치료 후 발생한 이상사례를 기반으로 한다.
b. 96주-144주의 시험에서 대상자는 에파비렌즈 + 이 약 + 엠트리시타빈 대신 에파비렌즈 + 이 약/엠트리시타빈 복합제를 투여받았다.
c. 발진 반응에는 발진, 박탈성 발진, 전신성 발진, 반점성 발진, 반구진성 발진, 소양증 발진 및 수포성 발진이 포함된다.
임상검사치 이상 : 이 시험에서 관찰된 임상검사치 이상은 일반적으로 이전 시험에서 나타난 것과 일치했다(표 5).
표 5. 시험 934(0-144주)에서 1% 이상 발생이 보고된 유의한 임상검사치 이상

a. 96주-144주의 시험에서 환자는 에파비렌즈와 이 약 + 엠트리시타빈 대신 에파비렌즈 + 테노포비르 DF/엠트리시타빈 복합제 치료를 받았다.
나. 치료 경험이 있는 HIV-1 감염 성인 환자
치료 후 발생한 이상반응 : 치료 경험 있는 대상자에서 나타난 이상반응은 구역, 설사, 구토 및 복부팽만과 같은 경증 내지 중등도의 위장 이상반응을 포함하며, 치료 경험이 없는 대상자에서 나타난 이상반응과 일반적으로 일치했다. 1% 미만의 대상자가 위장관계 이상반응으로 임상 시험을 중단했다(시험 907).
시험 907의 처음 48주 동안에 발생한 중등도부터 중증의 치료와 관련된 이상반응에 대한 요약 내용은 표 6에 나와 있다.
표 6 시험 907(0-48주)에서 3% 이상 발생이 보고된 치료 관련 이상반응a(등급 2-4)

a. 이상반응 빈도는 시험약과의 상관관계와 무관하게 모든 치료 관련 이상반응을 기반으로 한다.
b. 말초 신경병증은 말초 신경염 및 신경병증을 포함한다.
c. 발진 반응에는 발진, 가려움증, 반구진발진, 두드러기, 수포성발진 및 농포성발진 등이 있다.

임상검사치 이상 : 이 시험에서 관찰된 임상검사치 이상은 이 약 및 위약 치료 그룹에서 비슷한 빈도로 발생했다. 등급 3과 4 실험실적 이상반응의 요약 내용은 표 7에 나와 있다.
표 7 시험 907(0-48주)에서 이 약 치료군 중 1% 이상 발생이 보고된 등급 3/4 임상검사치 이상

다. 12세 이상 소아 HIV-1 감염 환자에 대한 임상시험
184명의 HIV-1 감염 소아 환자(2세 이상 18세 미만)에 대해 다른 항레트로바이러스제와 병용하여 48주간 이 약(N=93) 또는 위약/활성대조약(N=91) 치료를 진행한 2 건의 무작위 배정 임상시험(시험 321) 결과를 근거로 이상반응 평가가 이루어졌다. 이 약 치료를 받은 소아 환자에서의 이상반응은 성인에 대한 임상시험에서와 일관되게 나타났다.
만성 B형 간염 환자에 대한 임상시험
가. 만성 B형 간염 및 대상성 간 질환이 있는 성인 환자에 대한 임상 시험
치료 후 발생한 이상반응: 만성 B형간염 대상자에 대한 대조 임상시험(0102 및 0103)에서 48주간의 이중 맹검 기간 동안 이약 치료를 받은 대상자가 더 많이 구역을 경험했다(이 약 9% vs 아데포비어 디피복실 제제 2%). 이 약으로 치료를 받은 환자 중 5% 이상이 보고한 기타 치료 후 발생한 이상반응으로는 복통, 설사, 두통, 현기증, 피로, 코인두염, 요통, 피부 발진이 포함된다.
0102 및 0103 시험에서 이 약으로 치료하는 공개라벨 단계(48 - 384주)에서 2%의 대상자(13/585명)가 기저시점 대비 혈청 크레아티닌 0.5 mg/dL 상승으로 확인되었다.
이 시험에서 최대 384주 동안 이 약으로 지속적인 치료를 받은 대상자에서 내약성 프로파일의 유의한 변화는 관찰되지 않았다.
임상검사치 이상 : 48주간의 등급 3과 4 실험실적 이상반응의 요약 내용은 표 8에 나와 있다. 등급 3과 4 임상검사치 이상은 최대 384주 동안 이 약으로 지속적인 치료를 받은 대상자에서 나타난 이상반응과 유사했다.
표8. 시험 102와 103에서 이 약 치료 그룹에서 1% 이상 발생이 보고된 등급 3/4 실험실적 이상반응

치료 중 ALT 발적(관련 증상이 있거나 없으며, 혈청 ALT가 기준치의 2배 초과이고 정상 상한치의 10배 초과인 것으로 정의됨)의 전반적인 발생율은 이 약(2.5%)과 아데포비어(2%)간에 유사했다. ALT 발적은 일반적으로 치료 후 첫 4-8주 내에 나타났으며, HBV DNA 수치의 감소와 함께 발생했다. 대상부전의 징후를 보인 대상자는 없었다. 일반적으로 ALT 발적은 시험약을 변경하지 않아도 4-8주 이내에 해결된다.
만성 B형 간염과 라미부딘 내성을 가진 이 약 치료 환자에서 관찰된 이상반응은 다른 성인 대상 B형 간염 임상시험에서 관찰된 것과 일관되게 나타났다.
나. 만성 B형 간염 및 비대상성 간 질환이 있는 성인 환자에 대한 임상 시험
소규모의 무작위 이중 맹검, 활성 대조 시험(0108)에서 CHB와 비대상성 간 질환을 앓고 있는 환자를 최대 48주 동안 이 약 또는 기타 항바이러스 약물로 치료했다. 이 약 치료를 받은 45명의 환자가 중증도에 관계 없이 가장 자주 보고했던 치료 관련 이상반응은 복통(22%), 오심(20%), 불면증(18%), 가려움증(16%), 구토(13%), 현기증(13%), 발열(11%)이었다. 45명 대상자 중 2명(4%)은 48주간의 시험 기간 중 간 질환이 진행됨에 따라 사망했다. 45명의 대상자 중 3명(7%)은 이상반응으로 인해 치료를 중단했다. 45명의 대상자 중 4명(9%)은 혈청 크레아틴이 0.5 mg/dL 증가되었다(또한 1명은 48주 동안 혈청 인산이 2mg/dL 미만으로 되었다). 이러한 대상자 중 3명(등록 시점에 Child-Pugh 지수가 10 이상이고, MELD 지수가 14이상이었음)은 신장 손상이 악화되었다. 이 약와 비대상성 간 질환이 모두 신장 기능에 영향을 줄 수 있으므로, 이 모집단에서 이 약이 신장 손상에 미친 영향이 어느 정도인지 알아내기는 어렵다.
45명의 대상자 중 한 명은 48주의 시험기간 중 치료 시 간염 발적을 겪었다.
다. 12세 이상 소아 만성 B형 간염 환자에 대한 임상시험
106 명의 만성 B형 간염 소아(12세 이상 18세 미만) 환자를 대상으로 72주간 이 약(N=52) 또는 위약(N=54) 치료를 진행한 무작위배정 임상시험(시험 GS-US-174-0115)에서 이상반응 평가가 이루어졌다. 이 약 치료를 받은 소아 환자에서의 이상반응은 성인에 대한 임상시험에서와 일관되게 나타났다.
골밀도 평균 증가율은 이 약 치료군이 위약 치료군에 비해 낮았다.
2) 시판 후 경험
이 약 시판 후 사용 중 다음과 같은 이상반응이 확인되었다. 시판 후 이상반응은 불명확한 규모의 모집단에서 자발적으로 보고되기 때문에 항상 신뢰성 있게 발생율을 예측하거나 약물 투여에 대한 인과 관계를 입증하는 것이 가능하지 않을 수 있다.
- 면역계 장애
알레르기 반응(혈관부종 포함)
- 대사 및 영양 장애
유산증, 저칼륨증, 저인산혈증
- 호흡계, 흉부 및 종격 장애
호흡곤란
- 위장 장애
췌장염, 아밀라아제 증가, 복통
- 간담낭 장애
간지방증, 간염, 간 효소 증가(가장 일반적으로 AST 및 ALT 감마 GT)
- 피부 및 피하 조직 장애
발진
- 근골격계 및 결합 조직 장애
횡문근 융해증, 골연화증(골통으로 나타나며, 골절을 유발할 수 있음), 근육 약화, 근질환
- 신장 및 비뇨기 장애
급성 신부전, 신부전, 급성 세뇨관 괴사, 판코니 증후군, 근위 세뇨관증, 간질성 신염(급성인 경우 포함), 신장성 요붕증, 신부전, 크레아티닌 증가, 단백뇨, 다뇨증
- 일반 장애 및 투약 부위 병태
무력증
상기 신체기관 하에 나열된 다음의 이상반응은 근위 신장 세뇨관증의 결과로 발생할 수 있다: 횡문근 융해증, 골연화증, 저칼륨증, 근육 약화, 근질환, 저인산혈증
※ 국내 시판 후 조사 결과
국내에서 재심사를 위하여 6년 동안 746명의 만성 B형 간염 대상자를 대상으로 실시한 시판후 조사 결과, 이상사례의 발현율은 인과관계와 상관없이 11.66%(87/746명, 225건)로 보고되었다. 이 중 인과관계와 상관없는 중대한 이상사례 및 인과관계를 배제할 수 없는 중대한 약물이상반응은 발현 빈도에 따라 아래 표에 나열하였다.

또한, 인과관계와 상관없는 예상하지 못한 이상사례와 인과관계를 배제할 수 없는 예상하지 못한 약물이상반응은 발현 빈도에 따라 다음의 표에 나열하였다.

‧₊˚.⋆·ฺ.∗̥✩⁺˚ ੈ‧˚૮꒰˵• ﻌ •˵꒱აੈ✩‧₊˚ੈ*:゚*。.⋆·ฺᐝ.∗̥⁺˚





'약 효능효과, 부작용, 주의사항' 카테고리의 다른 글
| [약] 엘리델 크림1% 30g 효능 효과, 부작용, 이상반응, 주의사항 (0) | 2019.06.23 |
|---|---|
| [약] 액시마정 효능 효과, 부작용, 이상반응, 주의사항 (0) | 2019.06.23 |
| [약] 이소티논연질캡슐 효능 효과, 부작용, 이상반응, 주의사항 (0) | 2019.06.23 |
| [약] 비리어드정 효능 효과, 부작용, 이상반응, 주의사항 (0) | 2019.06.23 |
| [약] 명인트라조돈캡슐25mg 효능 효과, 부작용, 이상반응, 주의사항 (0) | 2019.06.23 |
| [약] 데파스정0.5mg 효능 효과, 부작용, 이상반응, 주의사항 (0) | 2019.06.22 |
| [약] 큐란정300mg 효능 효과, 부작용, 이상반응, 주의사항 (0) | 2019.06.22 |
| [약] 덱실란트디알캡슐30mg 효능 효과, 부작용, 이상반응, 주의사항 (0) | 2019.06.22 |